Maddeler tanecikli yapıda bulunurlar. Ancak atom ve moleküller çok küçük tanecikler olduğundan günümüzde geliştirilmiş mikroskoplarla bile görülmez ve bugünkü ölçü aletleri ile kütleleri tanılamaz. Atom ve moleküllerin birer tanelerinin yerine birer mollerinin kütleleri kullanılır.
Mol :
Avogadro sayısı (6,02.1023) kadar taneciğe 1 mol denir.
Örneğin;
- 6,02.1023 tane proton : 1 mol proton
- 6,02.1023 tane nötron : 1 mol nötron
- 6,02.1023 tane atom : 1 mol atom
- 6,02.1023 tane molekül : 1 mol molekül
- 6,02.1023 tane kalem : 1 mol kalem
Bağıl Atom Kütlesi :
Bir atomun kütlesinin diğer atomun kütlesinin kaç katı olduğunu belirten değere bağıl atom kütlesi denir.
Karbon eIementinin bir tane atomunun küt lesi 12 atomik kütle birimi (a.k.b) kabul edilip, diğer elementlerin birer atomlarının kütleleri karbon atomu ile kıyaslanarak bağıl atom kütlesi bulun muştur.
Elementlerin bağıl kütleleri kimyasal problemlerde belirtilir.
Örneğin;
Bir karbon atomunun kütlesi bir helyum atomunun kütlesinin 3 katı, bir magnezyum atomunun kütlesinin yarısı kadar olduğundan;
- 1 karbon atomu : 12 a.k.b
- 1 helyum atomu : 4 a.k.b
- 1 magnezyum atomu : 24 a.k.b dir.
Mol – Atom (Atom – gram) Kütlesi
Avogadro sayısı kadar atomun kütlesi 1 mol atomun kütlesine eşittir.
1 tane karbon atomunun kütlesi 12 a.k.b dir. 1 mol karbon atomunun kütlesi ise 12 gramdır. Yani 1 atom – gram karbon, 12 gramdır.
Örneğin;
1 tane Mg atomu : 24 a.k.b
1 mol Mg atomu : 24 gram
1 tane Mg atomu : 4.10-23 gram
1 mol Mg atomu : 6,02.1023 tane Mg atomu


- Buna göre verilen oksijenin kütleleri arasında | > Ill > Il ilişkisi vardır.
Gerçek Atom Kütlesi :
Herhangi bir elementin bir tane atomunun kütlesine denir. Her atom için sabit bir değer olup Avogadro sayısı ile çarpılırsa 1 mol atomunun kütlesine eşit olur.
Bir element için Avogadro sayısı değiştirilse bile gerçek atom kütlesi değişmez, ancak mol atom kütlesi değişir.
Örneğin;
Karbon (C) elementinin atom kütlesi 12 denildiğinde buradan şu anlamlar çıkarılmalıdır.
Karbon elementi molle ifade ediliyorsa;
- 1 mol karbon (C) atomu : 12 gramdır.
Karbon elementi tane ile ifade ediliyorsa;
- 1 tane karbon (C) atomu : 12 a.k.b dir.
Bir elementin gerçek atom kütlesi, mol atom kütlesinin Avogadro sayısına bölümü şeklinde de ifade edilebilir.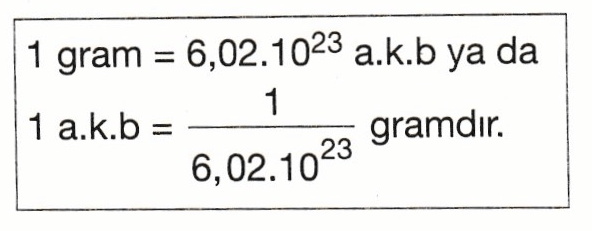
1 tane karbon (C) atomu 12 / 6,02.1023 gramdır.


Mol Molekül (Molekül – gram) Kütlesi :
Avogadro sayısı kadar molekülün kütlesine 1 mol molekülün kütlesi denir.
CO2’nin bağıl molekül kütlesi 44 a.k.b olduğundan, 44 gram CO2, 1 mol molekül CO2 dir.
Örneğin;
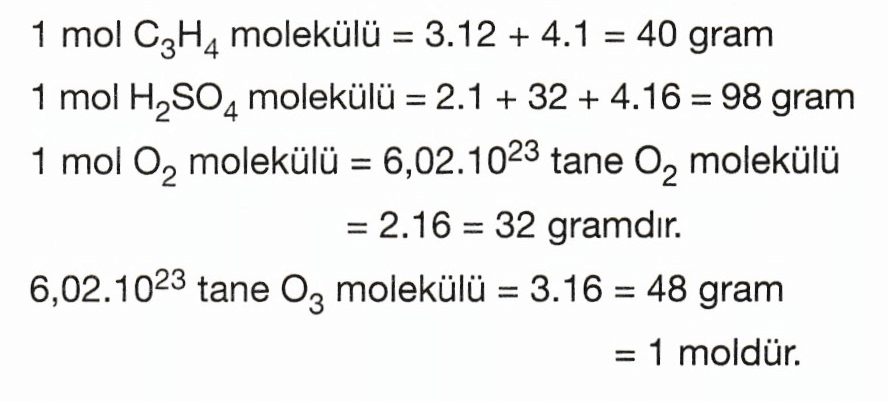
Gerçek Molekül Kütlesi :
 Bir tane molekülün kütlesine denir. Her molekül için sabit bir değerdir. 1 tane molekülün kütlesinin, Avogadro sayısı ile çarpımı o molekülün 1 molünün kütlesini verir.
Bir tane molekülün kütlesine denir. Her molekül için sabit bir değerdir. 1 tane molekülün kütlesinin, Avogadro sayısı ile çarpımı o molekülün 1 molünün kütlesini verir.

Gazların Molar Hacmi :
1 mol gazın kapladığı hacme molar hacim denir. Gazların hacmi içerisinde bulundukları kabın hacmine eşittir. Ortamın basınç ve sıcaklığına göre gazların kapladığı hacim değişebilir.
Aynı sıcaklık ve basınçta gazların eşit hacimlerinde eşit sayıda tanecik (molekül) bulunur. Bu ifadeye Avogadro hipotezi denir.
Sıcaklığın 0 ‘C , basıncın 1 atmosfer olduğu koşullara normal koşullar (N.K), sıcaklığın 25 ‘C, basıncın 1 atmosfer olduğu koşullara ise oda koşulları denir.
Bütün gazların birer molleri, normal koşullarda (N.K) 22,4 litre, oda koşullarında ise 24,5 litre hacim kaplar.
Örneğin;
- 1 mol H2 gazı molekülü;
- 2 gramdır.
- 6,02.1023 tane molekül içerir.
- N.K da 22,4 litre hacim kaplar.
- Oda koşullarında 24,5 litre hacim kaplar.
